2024年12月31日,中國科學(xué)院深圳先進技術(shù)研究院合成生物學(xué)研究所合成生物化學(xué)研究中心(以下簡稱“深圳先進院合成所生化中心”)羅小舟團隊和北京大學(xué)藥學(xué)院劉濤團隊在國際著名學(xué)術(shù)期刊《化學(xué)評論》(Chemical Reviews,影響因子51.4)聯(lián)合在線發(fā)表了題為“Genetic code expansion: recent developments and emerging applications”?的綜述文章,并被選為期刊封面(圖1)。文章從系統(tǒng)層面詳細概述了基因密碼子擴展技術(shù)(GCE)的現(xiàn)狀以及面臨的挑戰(zhàn)與機遇,并重點論述了其在合成生物學(xué)、生物機制研究和新型治療等前沿領(lǐng)域的應(yīng)用潛力。

文章上線截圖

圖1. 配圖入選Chemical Reviews雜志封面
(封面設(shè)計師:范仕蕓、劉怡寧)
長期以來,DNA和RNA一直被視為存儲和傳遞遺傳信息的分子,而蛋白質(zhì)則是生命活動的主力軍。然而,天然蛋白質(zhì)僅由20種天然氨基酸構(gòu)成,這一定程度上限制了蛋白質(zhì)的結(jié)構(gòu)與功能多樣性。如今,基因密碼子擴展(GCE)技術(shù)正在打破這一局限,為生命科學(xué)研究帶來全新可能。該技術(shù)通過引入正交的氨酰-tRNA合成酶(aaRS)/tRNA對,在活細胞甚至完整生物體內(nèi)的蛋白質(zhì)翻譯過程中,精準(zhǔn)地將非天然氨基酸(ncAA)定點引入蛋白質(zhì)。迄今,已有超過200種功能獨特的ncAA成功通過用于GCE技術(shù),其多樣的化學(xué)基團推動了分子生物學(xué)、合成生物學(xué)以及生物醫(yī)學(xué)領(lǐng)域的快速發(fā)展。GCE技術(shù)不僅拓展了蛋白質(zhì)的化學(xué)潛力,也為研究人員探索、操控和開發(fā)蛋白質(zhì)功能,以及創(chuàng)新治療手段提供了全新的工具。
本篇綜述全面回顧了GCE技術(shù)過去5年的最新進展。文章梳理了GCE技術(shù)的誕生過程、優(yōu)化方法及其廣泛應(yīng)用(圖2),詳述了科學(xué)家近年來在關(guān)鍵環(huán)節(jié)的突破,包括翻譯元件的優(yōu)化、正交aaRS/tRNA對篩選方法的改進以及ncAA的生物合成等策略(圖2)。此外,文章還深入探討了GCE技術(shù)的多領(lǐng)域創(chuàng)新性應(yīng)用,從新型生物材料的設(shè)計,到更高效的藥物遞送系統(tǒng),再到更優(yōu)的基因編輯工具與疫苗研發(fā)方法(圖2)。GCE技術(shù)也在合成生物學(xué)和基礎(chǔ)生物機制研究中展現(xiàn)出了強大的潛力(圖2)。如今,GCE技術(shù)已覆蓋從原核到真核的各個角落。未來,隨著該技術(shù)效率和正交性的進一步提升,以及更多功能性ncAA的成功開發(fā),GCE技術(shù)有望催生具備全新功能的復(fù)雜生物系統(tǒng),為生物學(xué)與醫(yī)學(xué)領(lǐng)域帶來更深遠的影響。
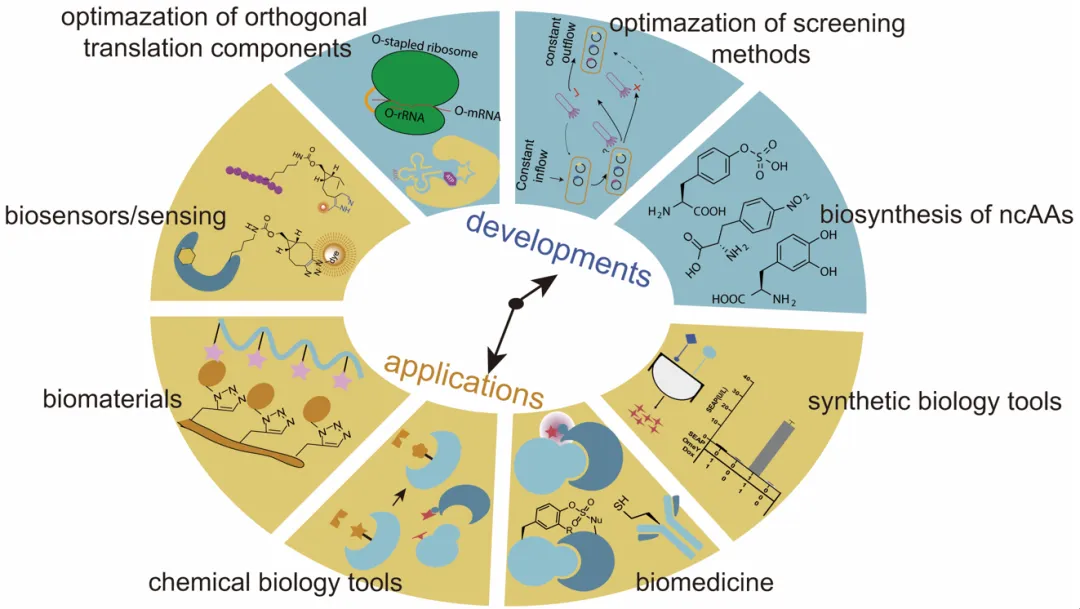
圖2. GCE技術(shù)的優(yōu)化與應(yīng)用
深圳先進院合成所生化中心羅小舟研究員和北京大學(xué)藥學(xué)院劉濤教授為本文的共同通訊作者。北京大學(xué)藥學(xué)院博士畢業(yè)生黃雨佳,深圳先進院合成所生化中心助理研究員張盼,北京大學(xué)藥學(xué)院碩士畢業(yè)生王浩宇為共同第一作者。中國科學(xué)院大學(xué)/深圳先進院合成所生化中心聯(lián)合培養(yǎng)在讀碩士生陳燕對本文撰寫也做出重要貢獻。本工作獲得了科技部重點研發(fā)計劃、國家自然科學(xué)基金項目、廣東省基礎(chǔ)與應(yīng)用基礎(chǔ)研究基金、深圳市自然科學(xué)基金的支持。
附件下載:


